Auf diesen Seiten möchten wir Ihnen einzellige Parasiten vorstellen. Diese bestehen - wie schon der Name sagt - aus nur einer Zelle. Sie vermehren sich im Körper des Wirtes und sind zumeist nur auf dem Mikroskop zu erkennen.
Kokzidien:
Kokzidien sind einzellige Lebewesen, die in der Darmwand ihrer Wirte leben und sich dort vermehren. Dabei befallen sie Zellen der Darmschleimhaut, die zerstört werden, wenn nach erfolgter Vermehrung durch Teilung die Nachfolgegeneration freigesetzt wird. Diese können entweder direkt neue Schleimhautzellen befallen oder sie gelangen mit dem Kot in die Umgebung (Oozysten). Hier werden sie entweder von ihrem spezifischen Wirt aufgenommen und der Kreislauf beginnt von neuem oder sie gelangen in einen Vertreter einer anderen Tierart, wo sie in die Körpergewebe (Milz, Leber, Herz, Lunge, Skelettmuskulatur) eindringen und dort in einem Ruhestadium verharren, bis das Gewebe von einem Endwirt aufgenommen wird und die Vermehrung gestartet werden kann.
Die Folge der Darmbesiedelung können bei Massenbefall Zerstörungen der Darmschleimhaut mit Entzündungen, Fieber und blutigem) Durchfall sein, außerdem Herabsetzung der Nahrungsausnutzung mit Minderernährung und Abmagerung. Die Besiedelung durch Wartestadien bleibt meist symptomlos.
Einen Sonderfall bilden die Gallengangskokzidien des Kaninchens. Diese zerstören bei starkem Befall die Schleimhaut der Gallengänge mit nachfolgender Entzündung und eventueller Verstopfung der Gallengänge, was zu Störungen der Leberfunktion und zu einer Vergrößerung der Leber führt.
Diagnostiziert wird ein Befall mit Kokzidien durch eine parasitologische Kotuntersuchung, wobei gleichzeitig ein Befall mit Rundwürmern festgestellt werden kann.
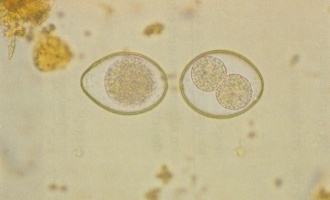
Kokzidien unter dem Mikroskop
Bekämpft werden Kokzidien nicht mit einer normalen Wurmkur, sondern mit speziellen Kokzidienpräparaten.
Toxoplasmen:
Toxoplasmen sind eng mit Kokzidien verwandt und durchlaufen einen ähnlichen Lebenszyklus, es gibt jedoch einige Besonderheiten:
Der Endwirt für Toxoplasmen ist allein die Katze, allerdings können fast alle anderen Tiere sowie der Mensch als Zwischenwirt fungieren. In der Katze parasitieren die Toxoplasmen in der Darmschleimhaut, in der sie sich vermehren und dann als Oozysten mit dem Kot ausgeschieden werden, bei allen anderen Tieren und beim Menschen kommt es zur Bildung von Gewebezysten in der Muskulatur oder in inneren Organen.
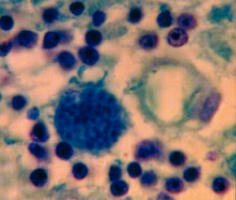
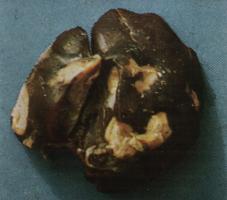
Toxoplasmenzyste im Gehirn
Hier ruhen die Toxoplasmen und warten ab, bis das Gewebe von einer Katze gefressen wird, denn nur dann können sie sich weiterentwickeln. Wird das zystenhaltige Gewebe von einem anderen Tier oder vom Menschen verzehrt, kommt es wiederum zur Zystenbildung. Bei der Katze bleibt der Befall meist unentdeckt, da nur etwa 3 Wochen lang Oozysten ausgeschieden werden. Danach bildet die Katze eine Immunität gegen Toxoplasmen aus, so dass sich die Erreger im Darm dieses Tieres nicht mehr vermehren können.
Die Oozysten sind nicht sofort infektionsfähig, sondern benötigen zuvor eine Phase der Weiterentwicklung in der freien Umgebung, die je nach Außentemperatur mindestens 2 Tage dauert. Daher ist eine Infektion über das Katzenklo nur in Ausnahmefällen möglich, nämlich dann, wenn das Klo nur selten gereinigt wird. Wenn die Entwicklung zu infektiösen Oozysten allerdings abgeschlossen ist, sind diese in der Umwelt sehr widerstandsfähig und können monatelang überdauern.
Der Befall eines erwachsenen Menschen äußert sich in grippe- oder erkältungsähnlichen Symptomen, wenn er nicht gänzlich symptomlos bleibt. Nur bei Menschen mit geschwächtem Immunsystem kann es zu Entzündungen des zentralen Nervensystems kommen. Soweit hat die Toxoplasmose keine große Bedeutung, kritisch wird allerdings ein Erstbefall bei schwangeren Frauen. In den letzten drei Schwangerschaftsmonaten verursachen Toxoplasmen, die über die Nabelschnur in das ungeborene Kind einwandern, schwerste Missbildungen der Augen oder des Gehirns. Diese Gefahr besteht allerdings nur, wenn sich die Schwangere erstmalig mit Toxoplasmen infiziert, wenn schon vor der Schwangerschaft eine Toxoplasmose durchgemacht wurde, besteht bei einer Neuinfektion keine Gefahr mehr für das Kind.
Die Übertragung erfolgt nur in den seltensten Fällen über Katzenkot, wie es von Humanmedizinern häufig behauptet wird, sondern die Hauptinfektionsquelle liegt im Verzehr von rohem oder nicht völlig durchgegartem Fleisch, aber auch eine Infektion über Rohmilchprodukte, verunreinigtes Gemüse oder durch Kontakt mit Katzenkot in Gartenerde oder Sandkisten ist möglich! Bei bestehender Schwangerschaft ist es also in keinem Fall erforderlich, eine Katze wegzugeben oder gar einschläfern zu lassen! Viel wichtiger ist die Vermeidung der anderen Infektionsquellen: Kein Verzehr von Tatar, Mett oder nicht durchgegarten Steaks, Handschuhe bei der Gartenarbeit und beim Säubern des Katzenklos, Reinigung des Katzenklos mindestens alle 2 Tage, Abdecken von Sandkisten usw.
Wenn eine Frau eine Schwangerschaft plant, empfiehlt sich folgendes Vorgehen: Man bittet seinen Arzt um eine Blutuntersuchung auf Antikörper gegen Toxoplasmose. Wenn Antikörper nachgewiesen werden, kann man das ganze Problem schon vergessen, denn dann besteht keine Gefahr mehr. Wenn aber keine Antikörper gefunden werden, kann man rechtzeitig vor der Schwangerschaft versuchen, eine Infektion durch reichlichen Verzehr von Mett, Tatar, Steaks und ähnlichem herbei-zuführen und dann noch einmal eine Blutuntersuchung durchführen lassen. Und dann gibt es wieder zwei Möglichkeiten:
Man kann feststellen, ob eine Katze schon einmal Kontakt mit Toxoplasmen gehabt hat, indem man das Blut des Tieres auf Antikörper untersucht. Um bei einem positiven Befund die Ausscheidung von Oozysten zu kontrollieren, kann man den Kot der Katze auf Toxoplasmose-Oozysten untersuchen, dabei ist ein positiver Befund allerdings sehr selten, da nur etwa 1 Prozent der freilaufenden Katzen Toxoplasmen-Oozysten ausscheiden.
Zur Verhinderung einer Infektion von Katzen empfiehlt sich die Vermeidung der Verfütterung entsprechender Futtermittel (rohes Fleisch und Rohmilchprodukte) sowie die Unterbindung des Freilaufens, um ie Aufnahme von zystenhaltigen Beutetieren zu verhindern. Allerdings muss man davon ausgehen, dass etwa 70 Prozent der Katzen infiziert sind.
Die Therapie einer Toxoplasmose bei der Katze erfolgt wie bei der Kokzidiose, ist aber in der Regel nicht notwendig, da die Oozystenauscheidung durch den Aufbau einer Immunität von allein nach etwa 3 Wochen aufhört und auch nach erneuter Infektion nicht wieder beginnt. Eine Therapie bei anderen Tieren ist nicht möglich.
Giardien:
Giardien sind frei bewegliche einzellige Parasiten, die sich an der Dünndarmwand von Hunden und Katzen anheften, was zu Entzündungen mit hartnäckigem, gelbem Durchfall führt. Von den Haustieren können Giardien auch auf den Menschen übertragen werden, eine Erkrankung, die zunehmend an Bedeutung gewinnt.
Der Nachweis von Giardien kann mit verschiedenen Methoden erfolgen:
- mikroskopische Untersuchung von frischem, noch warmem Kot: Dabei kann man die kreiselnden Bewegungen der Giardien sehen.
- normale parasitologische Kotuntersuchung nach Anreicherung: Dabei erscheinen die Dauerformen, die Zysten, die man unter dem Mikroskop sehen kann.
- Schnelltest: Hierbei wird eine Kotprobe mit einer Indikatorlösung vermischt und dann ein Teststäbchen eingetaucht. Bei einem positivem Ergebnis erscheint auf dem Stäbchen eine farbige Linie.
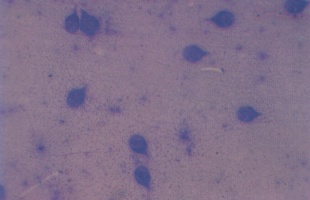
Giardien unter dem Mikroskop
Behandelt wird ein Befall mit Giardien mit einem Wirkstoff, der auch gegen Rundwürmer wirksam ist, so dass die Therapie zusammen mit einer Entwurmung durchgeführt werden kann.
Trichomonaden - Gelber Knopf der Tauben
Bei der Trichomonadenseuche handelt es sich um eine Aufzuchtkrankheit der Haus- und Wildtauben, seltener erkranken Hühner, Puten, Singvögel, Beos sowie Papageien und Sittiche. Sie wird hervorgerufen durch ein einzelliges Geißeltierchen, das als harmloser Mitbewohner in Schnabel und Speiseröhre der erwachsenen Tier lebt und bei diesen selten Krankheitssymptome (z. B. bei Immunschwäche)hervorruft. Die Alttiere übertragen der Erreger bei der Fütterung auf die Jungtiere, die mit ihrem noch in der Entwicklung begriffenen Immunsystem nicht in der Lage sind, mit den Trichomonaden fertig zu werden und daher erkranken. Es können sich unterschiedliche Krankheitsprozesse entwickeln:
- Rachen- und Kropftrichomonadose, mit über 70 % die häufigste Form, bei Altvögeln die einzige Form Auf der Schleimhaut von Rachen, Speiseröhre und Kropf bilden sich herdförmige, gelbe, linsen- bis walnussgroße, trocken-käsige Wucherungen. Wenn man diese ablöst, bleiben blutende Schleimhautwunden zurück. Als weitere Symptome zeigen sich Atemnot, Schluckbeschwerden, süßlicher Geruch der Atemnot, evtl. Tod durch Ersticken oder Verhungern.
- Nabeltrichomonadose, etwa 5 - 10 % der Fälle. Bei nestjungen Vögeln kann der Erreger über mit Futter oder Kropfmilch kontaminiertes Nistmaterial durch die noch offene Nabelpforte eindringen und derbe bis wachteleigroße Knoten bilden.
- Organtrichomonadose, 25 - 40 % der Erkrankungen. Wenn die Trichomonaden über den Nabel oder durch Schleimhautverletzungen im Kopfbereich in die Blutbahn eindringen, bilden sich scharf abgegrenzte, gelbliche Nekroseprozesse besonders in der Leber, aber auch In den Lungen, den Luftsäcken, in Herz, Bauchspeicheldrüse oder Gehirn. Als Symptome zeigen sich dabei hochgradig gestörtes Allgemeinbefinden und rascher Konditionsverlust sowie Durchfall und Atemnot.
Diagnostiziert wird eine Rachentrichomonadose häufig schon durch eine Untersuchung des Rachens, bei der die gelben Beläge auffallen. Außerdem kann man die Erreger aus Rachenabstrichen mikroskopisch nachweisen.
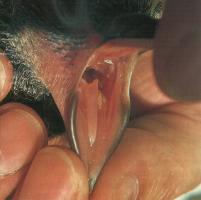 |
 |
| Gelber Knopf bei einer Jungtaube | Lebernekrosen durch Trichomonaden |
Vorbeugung und Therapie erfolgen auf die gleiche Weise: Es gibt Präparate, die für mehrere Tage über das Trinkwasser gegeben werden, es gibt auch ein Präparat in Tablettenform, das nur einmal, in schweren Fällen ein 2. Mal nach 5 Tagen gegeben wird, allerdings an jede Taube einzeln. Wichtig zur Vorbeugung ist die Behandlung der Alttiere bis etwa 10 Tage vor Brutbeginn.
Encephalitozoon caniculi - Encephalitozoonose des Kaninchens
Die Enzephalitozoonose wird durch den intrazellulär parasitierenden Erreger Encepahlitozoon (E.) cuniculi hervorgerufen. Zwar sind akute Krankheitsverläufe mit Todesfolge eher selten, doch können auch die meist subklinisch-latent verlaufenden Infektionen bereits Läsionen an den Nieren, im Gehirn und an anderen Organen hervorrufen.
Da durch molekularbiologische und immunologische Untersuchungen gleiche Erregergenotypen bei Mensch und Tier nachgewiesen werden konnten, muss E. cuniculi als Zoonoseerreger eingestuft werden
Während sich bei immunkompetenten Menschen Infektionen nahezu ausschließen lassen, stellt die Enzephalitozoonose für Menschen mit einem Immundefekt (z.B. Transplantatempfänger, HIV-positive Patienten) eine Gefahr dar. Bei ihnen kann sich eine Infektion als Binde- und Hornhautentzündung manifestieren oder als systemische Erkrankung mit Lungenentzündung, Nasennebenhöhlenentzündung, Harnwegsinfektion, Nierenentzündung, Hepatitis und/oder Bauchfellentzündung.
Kaninchen stellen auch für Kinder eine mögliche Gefahr dar, da diese zumeist sehr intensiven Körperkontakt mit den Tieren haben und ihr Immunsystem oftmals noch nicht vollständig ausgebildet ist.
Der Übertragungsmodus der Sporen von E. cuniculi ist noch nicht abschließend geklärt. Die Hauptausscheidung der Erregersporen erfolgt während bestimmter Infektionsstadien über den Harn. Dies kann zu einer Verunreinigung von Einstreu und Futter und somit zu einer peroralen Infektion weiterer Tiere führen. Außerdem wird von einer aerogenen (über die Atemluft) und einer vertikalen (transplazentar, über die Nabelschnur) Übertragung berichtet. Diese Infektionswege scheinen allerdings von untergeordneter Bedeutung zu sein.
E. cuniculi verursacht beim Kaninchen im Allgemeinen eine subklinisch-latente Infektion, die über Jahre bestehen kann. Als Ursachen für eine plötzliche Erregerausscheidung und einer daraus resultierenden klinisch manifesten Erkrankung wird eine Suppression des Immunsystems durch Stressfaktoren vermutet. Der akute Krankheitsverlauf ist vorwiegend durch zentralnervöse Störungen gekennzeichnet, darüber hinaus kommt es jedoch auch zu Niereninsuffizienzen und Augenveränderungen.
Die am häufigsten auftretenden neurologischen Symptome sind Gangunsicherheiten bis hin zu Kreisbewegungen und Rotationen um die Längsachse, Kopfschiefhaltung bis zu 180° sowie Augenzittern.
Patienten mit Niereninsuffizienz zeigen meist nur unspezifische Symptome, wie Appetitverlust, Austrocknung, Apathie und Gewichtsverlust. Selten wird von einem vermehrten Harndrang und vermehrter Wasseraufnahme berichtet, die gelegentlich mit durchnässtem Fell in der Anogenitalregion einhergehen.
Zunehmend häufiger wird eine Linsenentzündung des Auges (meist einseitig und mit fortschreitendem Verlauf) ohne Verhaltensänderungen oder Störungen des Allgemeinbefindens beschrieben. Es handelt sich dabei um einen reaktiven Prozess, der durch den Austritt von Linsenprotein nach Ruptur der vorderen Linsenkapsel verursacht wird. Klinisch sind neben einer deutlichen Irisentzündung mit starker Gefäßinjektion "weiße Massen" in der vorderen Augenkammer zu erkennen, die die Iris teilweise verdecken. Die Linsenentzündung ist bei den betroffenen Patienten oft der einzige klinische Hinweis auf eine Enzephalitozoonose und weist auf eine frühe intrauterine Infektion hin, als die Linsenkapsel noch sehr dünn oder noch gar nicht entwickelt war.
Außerdem wird von Herzmuskelläsionen berichtet, die entweder asymptomatisch bleiben oder auch zum plötzlichen Herztod führen können.
Seit einigen Jahren ist eine Therapie der Encephalitozoonose mit einem Antiparasitikum möglich. Dieses muss über 4 Wochen täglich gegeben werden. Zusätzlich wird meistens ein Antibiotikum eingesetzt.




